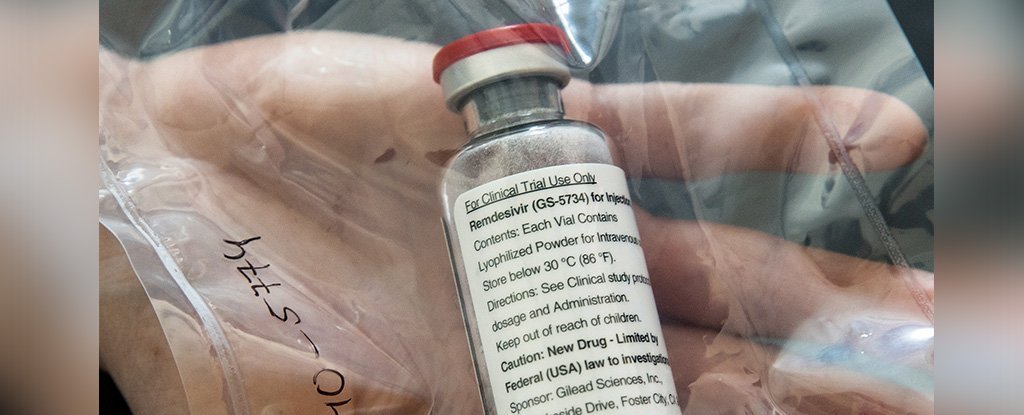
A Food and Drug Administration concedeu na quinta-feira a aprovação total ao medicamento antiviral remdesivir como tratamento para pacientes hospitalizados com COVID-19 , após autorização condicional concedida em maio.
Segundo a Gilead, foi o único tratamento específico para COVID-19 aprovado até agora sob um processo mais rigoroso.
No entanto, outros tratamentos receberam autorização para uso emergencial, embora essa aprovação possa ser revogada assim que a emergência de saúde pública desencadeada pela pandemia do coronavírus terminar.
Outros medicamentos, como o esteróide dexametasona, também estão sendo usados no combate ao COVID-19.
As ações da Gilead na Bolsa de Valores de Nova York saltaram 4% logo após o anúncio.
Saiba mais: Vacina COVID-19: Já estão testando injeções em crianças
A Europa e outros países como o Canadá também concederam aprovação temporária para o uso de remdesivir.
A droga inicialmente foi desenvolvida para tratar o Ebola, uma febre hemorrágica viral.
Veja também: Reguladores e especialistas dos EUA abordam questões polêmicas de estudos de vacinas
Remdesivir, que é administrado por injeção, foi um dos primeiros medicamentos a se mostrar relativamente promissor na redução do tempo de recuperação em alguns pacientes com coronavírus.
O medicamento é complexo de fabricar e é administrado por injeção, em vez de comprimido, houve dúvidas sobre se o suprimento poderia ser limitado inicialmente.
Fique por dentro: Será que algum dia chegaremos ao ‘Zero COVID-19’?
Mas sua eficácia na redução da taxa de mortalidade não foi comprovada.
Pode ser administrado a adultos e crianças com idade superior a 12 anos e peso superior a 40 quilos (88 libras) que necessitem de hospitalização para o tratamento de COVID-19, a doença causada pelo novo coronavírus.
Traduzido e adaptado por equipe Saibamais
Fonte: ScienceAlert





